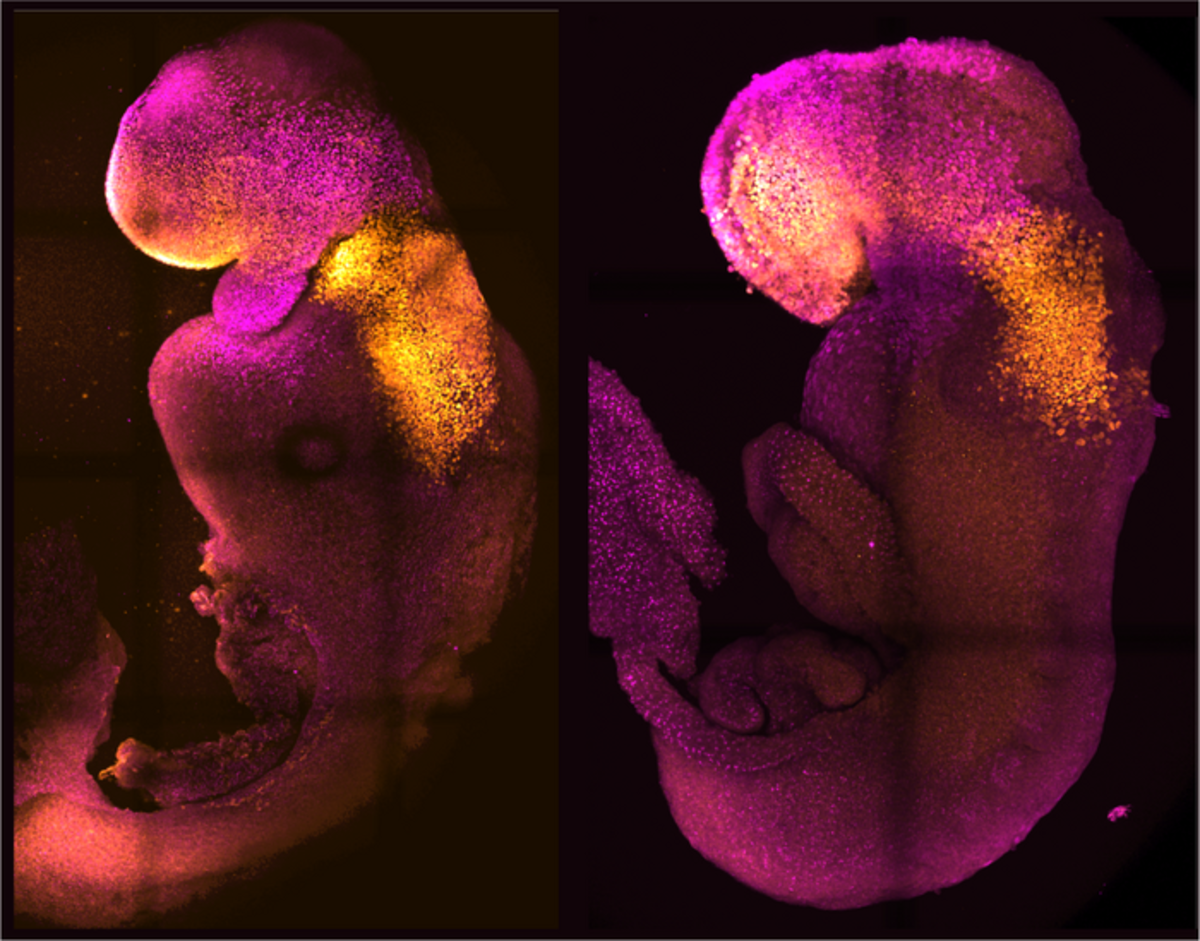
Badacze z University of Cambridge i California Institute of Technology, pod kierunkiem polskiej biolog, prof. Magdaleny Żernickiej-Goetz stworzyli z komórek macierzystych sztuczne mysie embriony, u których rozwinęły się mózgi i bijące serca. Pisze o tym w najnowszym numerze czasopismo "Nature". To dalszy ciąg prowadzonych od ponad dekady prac zmierzających do zrozumienia przyczyn, dla których niektóre embriony nie są w stanie zdrowo rozwinąć się do fazy płodowej. Są nadzieje, że te badania pomogą też w rozwoju technik tworzenia organów na zamówienie.
Embriony stworzono bez komórek rozrodczych. W laboratorium kierowanym przez prof. Żernicką-Goetz wykorzystano natomiast trzy rodzaje komórek macierzystych, czyli takich, które mogą rozwijać się w różne tkanki ciała. Naukowcy zmodyfikowali aktywność pewnych genów i stworzyli warunki, które pozwoliły tym komórkom oddziaływać i "dogadywać" się ze sobą. Komórki macierzyste stworzyły struktury, które przeszły przez kolejne fazy rozwoju do chwili, kiedy w embrionach pojawiły się zaczątki mózgów i bijące serca, a także pęcherzyki żółtkowe, które przez pierwsze tygodnie zapewniały im odżywianie. To najbardziej zaawansowane stadium sztucznych, utworzonych z komórek macierzystych embrionów, do którego nauce udało się do tej pory doprowadzić.
Za najważniejsze osiągnięcie autorzy pracy uznają sukces w tworzeniu mózgu, zwłaszcza jego przedniego obszaru. To otwiera nowe możliwości badań mechanizmu rozwoju tkanki nerwowej. Pokazaliśmy, że wyłączenie genu, o którym wiemy, że ma kluczowe znaczenie dla rozwoju tej tkanki, powoduje u sztucznych embrionów podobne zaburzenia, jak u zwierząt niosących taką mutację - mówi prof. Żernicka-Goetz. To otwiera drogę do badania wielu innych genów, których wpływu na tworzenie się tkanki nerwowej nie znamy. Nasz model embrionu myszy nie tylko ma mózg ale i bijące serce, kluczowe elementy ciała - dodaje Żernicka-Goetz. To niewiarygodne, że udało nam się do tego dojść. Nasze środowisko marzyło o tym od lat, pracowaliśmy nad tym od dekady, wreszcie zdołaliśmy tego dokonać.
By ludzki embrion mógł się właściwie ukształtować, niezbędne jest współdziałanie tkanek, które utworzą jego ciało, z tymi, które połączą go z matką. W pierwszym tygodniu po zapłodnieniu tworzą się trzy grupy komórek. To komórki tworzące ciało embrionu, komórki dające początek pęcherzykowi żółtkowemu, który zapewnia mu środowisko wzrostu i odżywienie, wreszcie komórki, które rozwiną łożysko łączące go z organizmem matki, zapewniające i oddychanie, i odżywianie. Badania wskazują na to, że wiele ciąż kończy się właśnie w okresie, kiedy te tkanki powinny zacząć wymieniać się sygnałami mechanicznymi i chemicznymi. Ten wczesny okres jest podstawą wszystkiego, co potem podczas ciąży się dzieje. Jeśli wtedy coś pójdzie nie tak, ciąża nie zakończy się sukcesem - podkreśla pierwsza autorka pracy. By stworzyć sztuczny embrion badacze umożliwili rozwój trzem grupom komórek macierzystych, z których każda podjęła jedno z tych kluczowych zadań.
Jak mówi prof. Żernicka-Goetz, która przybyła do Wielkiej Brytanii w 1990 roku, po studiach na Uniwersytecie Warszawskim, a ostatnio pracuje także w Kalifornii, lata pracy zespołu zmierzały do stworzenia warunków do badań tych wczesnych etapów ciąży, by możliwe było ustalenie przyczyn jej niepowodzeń. Stworzenie sztucznego embrionu z komórek macierzystych daje nam dostęp do rozwijających się struktur, do których ze względu na zagnieżdżenie w organizmie matki, nie mamy normalnie dostępu. To pozwala nam manipulować genami tak, by można było poznać ich rolę w procesach rozwoju - dodaje polska badaczka. Ten okres życia człowieka jest tak zagadkowy, że możliwość obserwacji i wpływu w laboratorium na poszczególne grupy komórek, poznawania co może zawieść, jest czymś szczególnym - dodaje Żernicka-Goetz.
Autorzy pracy przygotowują się do stworzenia analogicznego modelu w oparciu o ludzkie komórki macierzyste, by móc badać mechanizmy niemożliwe do obserwacji w przypadku rzeczywistych embrionów. Liczą na to, że ewentualny sukces pomoże też w przyszłym tworzeniu syntetycznych organów do transplantacji.